5. juulil käivitas Novo Nordisk Hiinas CagriSema süstimise III faasi kliinilise uuringu, mille eesmärk on võrrelda CagriSema süstimise ohutust ja efektiivsust semeglutiidiga rasvunud ja ülekaalulistel patsientidel Hiinas.
CagriSema süstimine on Novo Nordiski poolt väljatöötamisel olev pikatoimeline kombineeritud ravi, mille põhikomponentideks on GLP-1 (glükagoonilaadne peptiid-1) retseptori agonist smeglutiid ja pikatoimeline amüliini analoog kagrilintiid.CagriSema süsti võib manustada subkutaanselt üks kord nädalas.
Esmane eesmärk oli võrrelda CagriSemat (2,4 mg/2,4 mg) semeglutiidi või platseeboga üks kord nädalas subkutaanselt.Novo Nordisk avalikustas 2. staadiumi diabeedi raviks mõeldud CagriSema uuringu tulemused, mis tõestasid, et CagriSema hüpoglükeemiline toime on parem kui semeglutiidil ning ligi 90% katsealustest on saavutanud HbA1c eesmärgi.
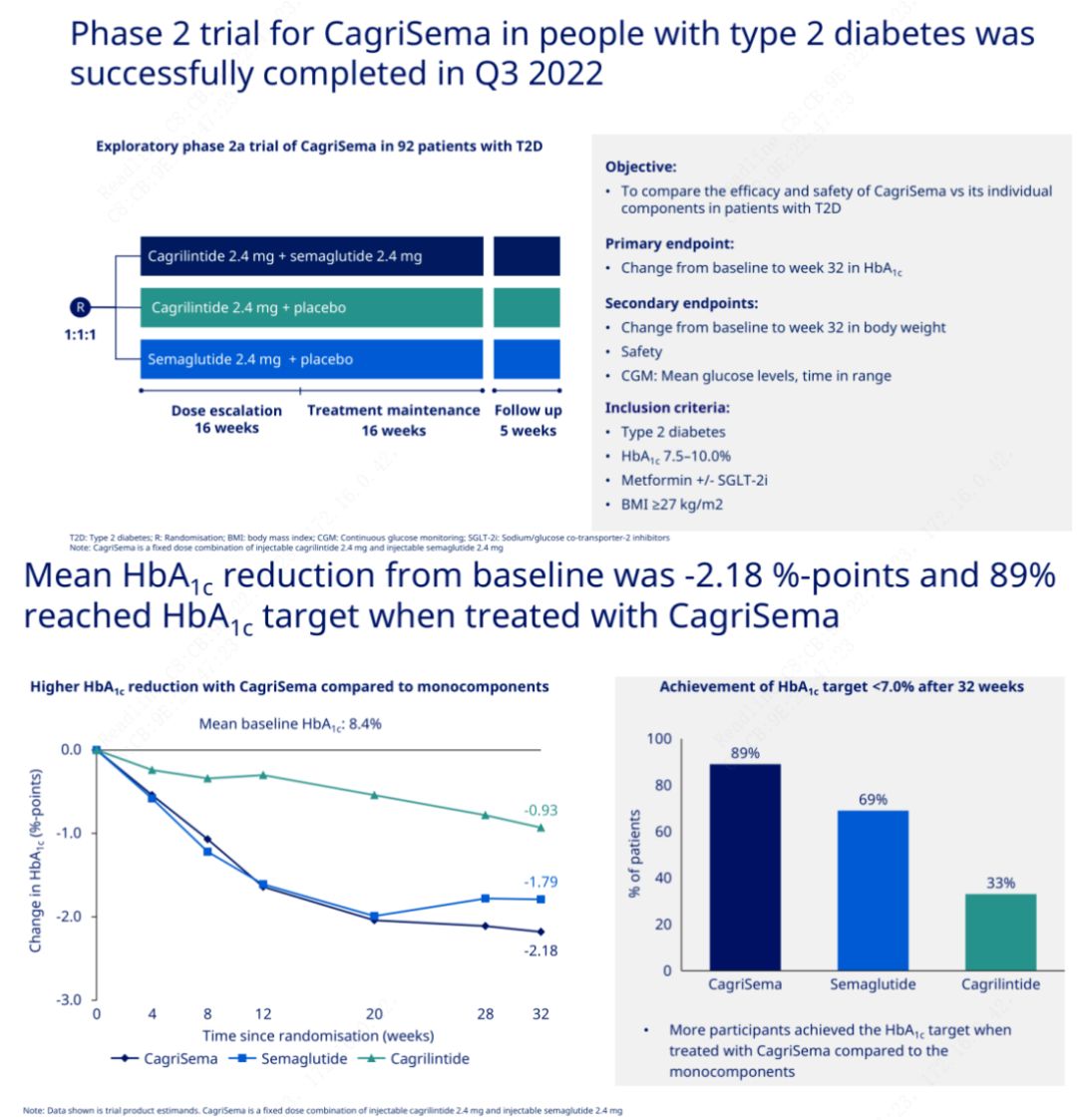
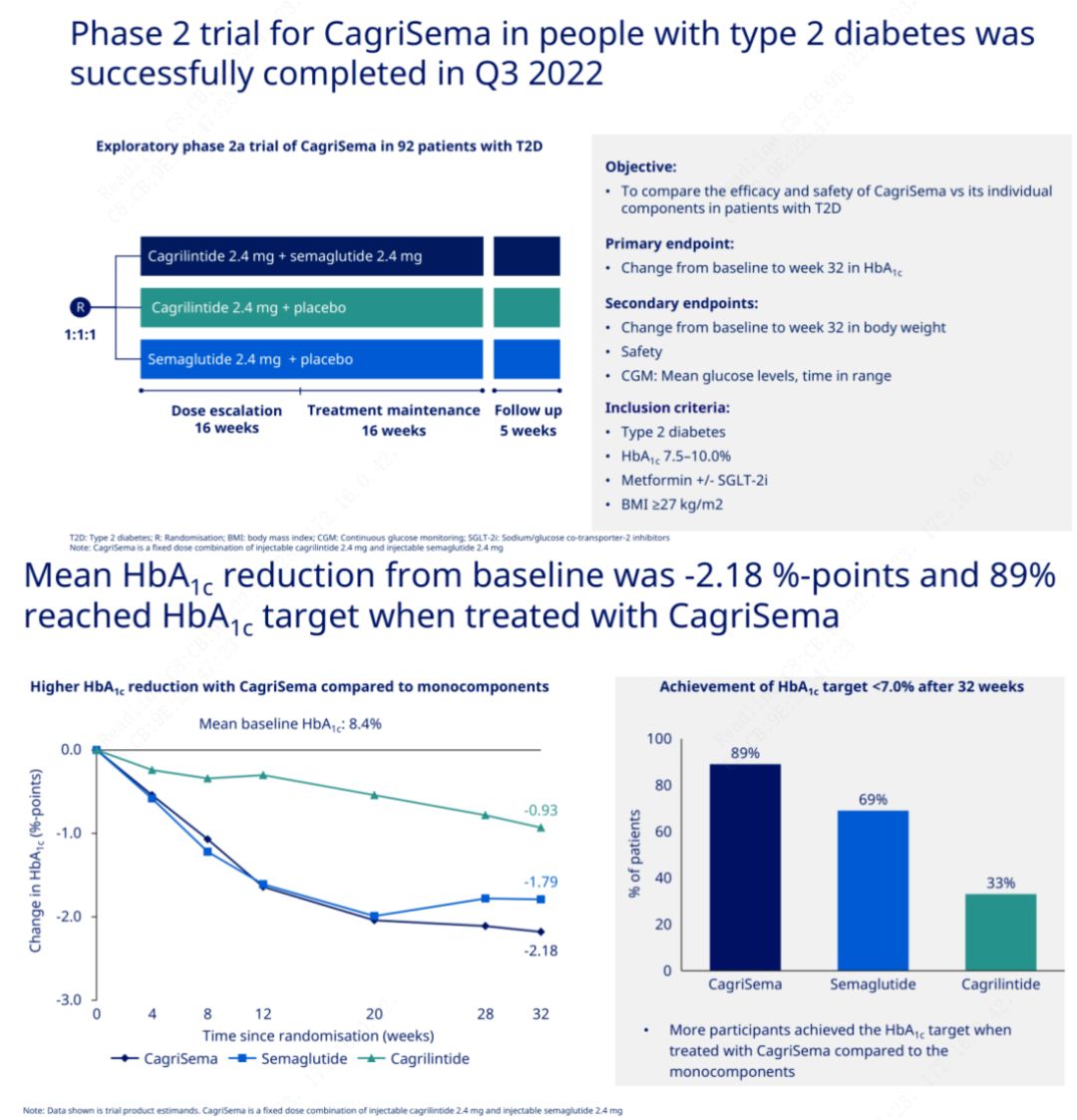
Andmed näitasid, et lisaks olulisele hüpoglükeemilisele toimele ületas CagriSema süstimine kaalulanguse osas oluliselt semeglutiidi (5,1%) ja kagrilintiidi (8,1%) kaalulangusega 15,6%.
Uuenduslik ravim Tirzepatiid on maailma esimene heakskiidetud iganädalane GIP/GLP-1 retseptori agonist.See ühendab kahe inkretiini toimed üheks molekuliks, mida süstitakse kord nädalas, ja see on uus klass 2. tüüpi diabeedi raviks.USA Toidu- ja Ravimiamet (FDA) kiitis tirtsepatiidi heaks 2022. aasta mais, et parandada II tüüpi diabeediga täiskasvanute glükeemilist kontrolli (toidu ja füüsilise koormuse alusel) ning praegu on see heaks kiidetud Euroopa Liidus, Jaapanis ja teistes riikides.
5. juulil teatas Eli Lilly III faasi uuringust SURPASS-CN-MONO ravimite kliiniliste uuringute registreerimise ja teabe avalikustamise platvormi kohta II tüüpi diabeediga patsientide raviks.SURPASS-CN-MONO on randomiseeritud, topeltpime, platseebokontrolliga III faasi uuring, mille eesmärk on hinnata tirtsepatiidi monoteraapia efektiivsust ja ohutust võrreldes platseeboga II tüüpi diabeediga inimestel.Uuringusse plaaniti kaasata 200 II tüüpi diabeediga patsienti, kes ei võtnud 90 päeva jooksul enne 1. visiiti ühtegi diabeediravimit (välja arvatud teatud kliinilistes olukordades, nagu äge haigus, haiglaravi või plaaniline operatsioon, lühiajaline (≤14). päevad) insuliini kasutamine).
2. tüübi diabeet peaks heakskiidu saama sel aastal
Eelmisel kuul avaldati SURPASS-AP-Combo uuringu tulemused 25. mail kassahiti ajakirjas Nature Medicine.Tulemused näitasid, et võrreldes glargiiniinsuliiniga näitas Tirzepatiid Aasia ja Vaikse ookeani piirkonnas (peamiselt Hiinas) 2. tüüpi diabeediga patsientide populatsioonis paremat HbA1c ja kehakaalu langust: HbA1c vähenemine kuni 2,49% ja kaalulangus kuni 7,2 kg. (9,4%) 40. ravinädalal oli vere lipiidide ja vererõhu oluline paranemine ning üldine ohutus ja talutavus head.
SURPASS-AP-Combo 3. faasi kliiniline uuring on Tirzepatide esimene uuring, mis viidi läbi peamiselt Hiina 2. tüüpi diabeediga patsientidel, mida juhtis Pekingi ülikooli rahvahaigla professor Ji Linong.SURPASS-AP-Combo on kooskõlas ülemaailmse SURPASS-i uuringute seeria tulemustega, mis tõestavad veelgi, et Hiina patsientide diabeedi patofüsioloogia on kooskõlas ülemaailmsete patsientide omaga, mis on aluseks uute ravimite samaaegsele uurimisele ja väljatöötamisele. Hiinas ja maailmas ning pakub ka kindlat tõendusmaterjali selle kohta, et Hiina patsientidele antakse võimalus kasutada võimalikult kiiresti uusimaid diabeediravi ravimeid ja nende kliinilist kasutamist Hiinas.
Postitusaeg: 18. september 2023

